- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:32.
- Zuletzt bearbeitet 2025-01-22 16:55.
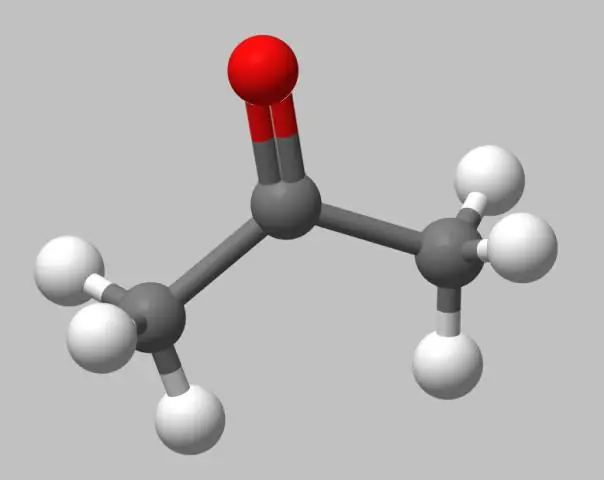
Kugel-Stick-Modelle . Kugel-Stick-Modelle sind nicht so realistisch wie raumfüllend Modelle , weil die Atome als Kugeln mit Radien dargestellt werden, die kleiner sind als ihre Van-der-Waals-Radien. Die Bindungsanordnung ist jedoch leichter zu erkennen, da die Bindungen explizit als Stöcke.
Anschließend kann man sich auch fragen, was stellt das Kugel-Stab-Modell dar?
In der Chemie ist die Kugel-Stick-Modell ist ein molekulares Modell einer chemischen Substanz, die sowohl die dreidimensionale Lage der Atome als auch die Bindungen zwischen ihnen anzeigen soll. Die Atome sind typischerweise repräsentiert durch Kugeln, verbunden durch Stäbe, die vertreten die Anleihen.
Und wie unterscheidet sich ein raumfüllendes Modell von einem Kugel-Stab-Modell? Kugel- und Stockmodelle sind dreidimensional Modelle wobei Atome durch Sphären von. dargestellt werden unterschiedlich Farben und Bindungen werden repräsentiert durch Stöcke zwischen den Kugeln. Raumfüllende Modelle sind ähnlich wie Kugel- und Stockmodelle , dass sie dreidimensional sind Modelle die Atome als farbige Kugeln darstellen.
Warum ist das Kugel-Stab-Modell hier nicht genau?
Die Kugel- und Stockmodell ist nicht ein wahr Darstellung der Struktur von Kaliumsulfid. 3.3) Schwefel kann auch kovalente Bindungen eingehen. 3.6) Ionische Verbindungen wie Kaliumsulfid haben hohe Siedepunkte und leiten Elektrizität, wenn sie in Wasser gelöst werden.
Ist Wasser polar oder unpolar?
Wasser (H2O) ist Polar - wegen der gebogenen Form des Moleküls. Die Form bedeutet, dass der größte Teil der negativen Ladung des Sauerstoffs auf der Seite des Moleküls und die positive Ladung der Wasserstoffatome auf der anderen Seite des Moleküls liegt. Dies ist ein Beispiel für Polar - kovalente chemische Bindung.
Empfohlen:
Wie lautet die Formel eines unpolaren Moleküls mit unpolaren Bindungen?

(1), (3) H2O und NH3 sind Moleküle, die polare kovalente Bindungen enthalten, aber ihre Elektronenverteilungen sind nicht symmetrisch. (4) H2 ist ein unpolares Molekül mit einer symmetrischen Elektronenverteilung, aber die Bindung zwischen den Wasserstoffatomen ist unpolar kovalent
Kann eine winzige Kugel mehr Schwung haben als ein riesiger Lastwagen?

Eine winzige Kugel kann mehr Schwung haben als ein riesiger LKW. Ein fahrendes Auto hat Schwung. Wenn er sich doppelt so schnell bewegt, ist sein Schwung doppelt so groß
Welche zwei Substanzen bilden das Rückgrat des DNA-Moleküls?

Expertenantworten info DNA oder Desoxyribonukleinsäure ist eine Doppelhelix mit einem Rückgrat, das aus abwechselnden Molekülen der Desoxyribose besteht, einem Zucker mit fünf Kohlenstoffatomen mit der chemischen Formel C5H10O4 und Phosphatmolekülen, einem anorganischen Salz mit der Formel PO4
Ist eine Kugel und ein Kreis dasselbe?

Obwohl sowohl Kugel als auch Kreis rund sind, unterscheiden sich beide voneinander. Wenn wir einen Fußball und ein Rad vergleichen, können wir den Unterschied zwischen ihnen verstehen. Eine Kugel ist ein dreidimensionales Objekt, während ein Kreis ein zweidimensionales Objekt ist
Erstreckt sich ein Codon von einem Ende eines tRNA-Moleküls?

Es erstreckt sich von einem Ende eines tRNA-Moleküls. Es ist die Grundeinheit des genetischen Codes. Es besteht aus drei Nukleotiden. Es kodiert nie für mehr als eine Aminosäure
