
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:32.
- Zuletzt bearbeitet 2025-01-22 16:55.
Die vier Quantenzahlen verwendet, um die zu beschreiben Elektronen sind n=2, ℓ=1, m=1, 0 oder -1 und s=1/2 (die Elektronen parallele Spins haben).
Und was beschreiben die vier Quantenzahlen über ein Elektron?
Um vollständig beschreiben ein Elektron in einem Atom, vier Quantenzahlen werden benötigt: Energie (n), Drehimpuls (ℓ), magnetisches Moment (ml) und Spin (mS). Der erste Quanten Nummer beschreibt das Elektron Hülle oder Energieniveau eines Atoms.
Wie findet man in ähnlicher Weise die Quantenzahl der Elektronen? So bestimmen Sie die Anzahl der Elektronen mit Quantenzahlen
- Zähle die vollen Orbitale.
- Fügen Sie die Elektronen für jedes volle Orbital hinzu.
- Identifizieren Sie die durch die Winkelquantenzahl angezeigte Unterschale.
- Fügen Sie die Elektronen aus den vollständigen Unterschalen hinzu.
- Fügen Sie die Elektronen aus vollen Unterschalen zu denen aus vollen Orbitalen hinzu.
- Finden Sie die legitimen Werte für die magnetische Quantenzahl.
Auch zu wissen, was sind die vier Quantenzahlen?
In Atomen gibt es insgesamt vier Quantenzahlen: die Hauptquantenzahl (n), das Orbital Drehimpulsquantenzahl (l), die magnetische Quantenzahl (ml) und das Elektron Spinquantenzahl (mS).
Was ist eine Unterschale?
EIN Unterschale ist eine Unterteilung von Elektronenschalen, die durch Elektronenorbitale getrennt sind. Unterschalen sind mit s, p, d und f in einer Elektronenkonfiguration bezeichnet.
Empfohlen:
Wie hängt die Elektronenkonfiguration mit den Quantenzahlen zusammen?
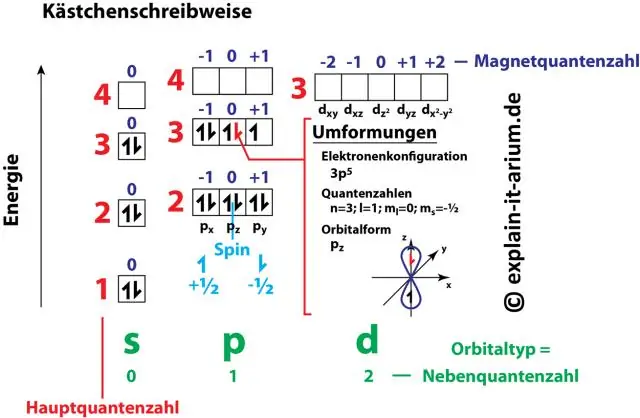
Die Zahlen- und Buchstabenpaare in einer Elektronenkonfiguration repräsentieren zwei der vier Quantenzahlen des Elektrons. Diese Quantenzahlen geben uns mehr Informationen über die Eigenschaften von Elektronen und ihren Orbitalen. Die Hauptquantenzahl (n) sagt uns das Energieniveau eines Elektrons und seine Größe
Was sind die sechs wesentlichen Elemente der Geographie, wie sie vom Nationalen Rat für Geographische Bildung definiert wurden?

Die sechs wesentlichen Elemente der Geographie (d. h. die Welt in räumlicher Hinsicht, Orte und Regionen, physikalische Systeme, menschliche Systeme, Umwelt und Gesellschaft sowie Verwendungen der Geographie) identifizieren und anwenden, einschließlich der spezifischen Begriffe für jedes Element
Wie lauten alle Formeln für Mathematik?

Liste der mathematischen Formeln Bereiche. Quadrat. `A=l^2` Volumen. Würfel. `V=s^3` Funktionen und Gleichungen. Direkt proportional. `y = kx` `k = y/x` Exponenten. Produkt. `a^mxxa^n=a^(m+n)` Radikale. Multiplikation. `root(n)(x)xxroot(n)(y)=root(n)(x xx y)` Trigonometrie. Trigonometrie-Verhältnisse. Geometrie. Die polyedrische Formel von Euler. Vektoren. Notation
Wie lauten die Formeln für arithmetische und geometrische Folgen?

Wenn Sie sich andere Lehrbücher oder online ansehen, werden Sie möglicherweise feststellen, dass sich ihre geschlossenen Formeln für arithmetische und geometrische Folgen von unseren unterscheiden. Insbesondere könnten Sie die Formeln an=a+(n'1)d a n = a + (n 1) d (arithmetisch) und an=a⋅rn'1 a n = a ⋅ r n − 1 (geometrisch)
Wie lauten die Buchstaben für Magnesium?

Magnesium: das Wesentliche Name: Magnesium. Symbol: Mg. Ordnungszahl: 12. Relative Atommasse (Ar): 24.305 Bereich: [24.304, 24.307] Standardzustand: fest bei 298 K. Aussehen: silbrig-weiß
