- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:32.
- Zuletzt bearbeitet 2025-01-22 16:55.
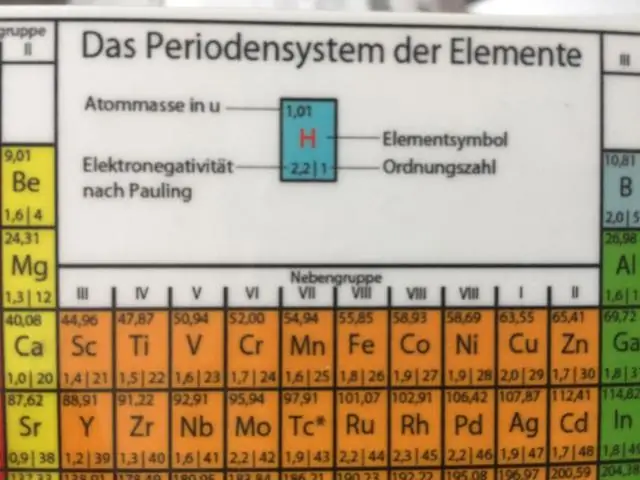
Isotope werden zuerst durch ihr Element und dann durch die Summe der vorhandenen Protonen und Neutronen definiert. Kohlenstoff-12 (oder 12C) enthält sechs Protonen, sechs Neutronen und sechs Elektronen; daher hat es eine Massenzahl von 12 amu (sechs Protonen und sechs Neutronen).
Wie entsteht hier ein Isotop?
Isotope sind Atome desselben Elements, die eine unterschiedliche Anzahl von Neutronen, aber die gleiche Anzahl von Protonen und Elektronen haben. Radioaktiv (instabil) Isotope Kerne haben, die im Laufe der Zeit spontan zu zerfallen Form Sonstiges Isotope.
Zweitens, was sind 3 Beispiele für Isotope? Einige Beispiele von stabil Isotope sind Isotope von Kohlenstoff, Kalium, Calcium und Vanadium. Radioaktiv Isotope haben eine instabile Kombination von Protonen und Neutronen, also haben sie instabile Kerne. Denn diese Isotope sind instabil, zerfallen und können dabei Alpha-, Beta- und Gammastrahlen aussenden.
Was ist dementsprechend Isotop und Beispiel?
Definition von Isotope . Elemente werden durch die Anzahl der Protonen im Atomkern definiert. Zum Beispiel , ein Atom mit 6 Protonen muss Kohlenstoff sein und ein Atom mit 92 Protonen muss Uran sein. Die Atome fast aller Elemente enthalten neben Protonen auch Neutronen.
Was ist ein Isotopensymbol?
Die nukleare Symbol besteht aus drei Teilen: dem Symbol des Elements, die Ordnungszahl des Elements und die Massenzahl des spezifischen Isotop . Hier ist ein Beispiel für einen nuklearen Symbol : Das Element Symbol , Li, ist das für Lithium. Die Anzahl der Protonen und Neutronen im Atomkern.
Empfohlen:
Wie führt man in Fallout 4 ein Kabel von einem Generator aus?

Bauen Sie einfach einen kleinen Generator und dann einen Gegenstand, der Strom benötigt (wie das Siedler-Sender-Ding). Gehen Sie zum Generator und Sie sollten unten eine Option zum Verlegen eines Kabels sehen. Drücken Sie X, um den Draht am Generator zu starten, gehen Sie zu dem mit Strom versorgten Element, drücken Sie X und der Draht wird automatisch vervollständigt. Voila, Macht
Wie führt man Operationen mit ganzen Zahlen durch?

Ganzzahlen sind ganze Zahlen, sowohl positive als auch negative. Sie können mit ihnen vier grundlegende mathematische Operationen durchführen: Addition, Subtraktion, Multiplikation und Division. Wenn Sie ganze Zahlen hinzufügen, denken Sie daran, dass positive ganze Zahlen Sie auf der Zahlengeraden nach rechts und negative ganze Zahlen nach links auf der Zahlengeraden bewegen
Wie führt man eine sinusförmige Regression auf einem Taschenrechner durch?
VIDEO Wie berechnet man hiervon die sinusförmige Regression? Sinusförmige Regression . Passen Sie die Werte von A, B, C und D im an Gleichung y = A*sin(B(x-C))+D um a. zu machen sinusförmig Kurvenanpassung an einen bestimmten Satz von zufällig generierten Daten.
Wie führt man ein Kalorimeter-Experiment durch?

Basiskalorimeterexperiment: Wärmeübertragung von Wasser. Messen Sie die Masse des leeren Kalorimeters mit einer Waage. Auf einer Datentabelle aufzeichnen. Gießen Sie kaltes Wasser – kein Eis – in das Kalorimeter, bis es zu einem Drittel gefüllt ist
Wie führt man einen TLC-Test durch?

Schneiden Sie das DC-Blatt in Streifen von ca. 2 cm x 7 cm. Zeichnen Sie eine Bleistiftlinie auf der kurzen Seite, etwa 0,5 cm von der Unterseite entfernt. Verwenden Sie keinen Stift, da sich die Tinte im organischen Lösungsmittel auflöst und sich ausscheidet und Ihre Ergebnisse verdeckt oder verunreinigt. Gießen Sie das/die zu testende(n) Lösungsmittel(n) in den Glasbehälter
