
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:32.
- Zuletzt bearbeitet 2025-01-22 16:55.
In dem Bohr-Modell , wird das Elektron als Teilchen in festen Bahnen um den Kern behandelt. Schrödingers Modell (Quantenmechanik Modell ) ermöglichte es dem Elektron, den dreidimensionalen Raum zu besetzen. Es brauchte daher drei Koordinaten oder drei Quantenzahlen, um die Verteilung der Elektronen im Atom zu beschreiben.
In ähnlicher Weise kann man sich fragen, wie sich Schrödingers Modell von Bohrs Quizlet unterscheidet?
Bohrs Modell zeigt die Elektronen, die sich als kreisförmige "Bahnen" um den Kern bewegen. Schrödingers Modell zeigt die Elektronen, die sich in wellenartigen Bewegungen um den Kern bewegen, die als "Orbitale" bezeichnet werden. Unterschiedlich Atome haben unterschiedlich Elektronenkonfigurationen, also geben sie a unterschiedlich Spektren des Lichts.
Was ist das Schrödinger-Modell? Ein leistungsfähiges Modell des Atoms wurde von Erwin. entwickelt Schrödinger im Jahr 1926. Die Schrödingermodell nimmt an, dass das Elektron eine Welle ist und versucht, die Regionen im Raum, Orbitale, zu beschreiben, in denen Elektronen am wahrscheinlichsten zu finden sind.
Wie hat Schrödinger einfach Bohrs Modell verändert?
In dem Bohr-Modell , die Elektronen sind Teilchen, die nur bestimmte Bahnen fester Energie um den Kern besetzen Schrödinger-Modell verhalten sich die Elektronen als stehende Wellen, die mit größerer Wahrscheinlichkeit in einigen Raumregionen (Orbitalen) sind als in anderen.
Was ist die Ähnlichkeit und der Unterschied zwischen dem Bohr-Modell und dem quantenmechanischen Modell?
Die Bohr-Modell behandelt die Elektronen mit gleichem Wert als entartet, d. h. mit gleicher Energie. Positionen, die von Elektronen besetzt sind: Die wichtigsten Ähnlichkeit zwischen die Zwei Modelle ist, dass in beiden Elektronen unterschiedlich Abstände vom Kern, entsprechend unterschiedlich Energien.
Empfohlen:
Wie unterscheidet sich tholeiitischer Basalt von den meisten vulkanischen Gesteinen?

Gesteine der tholeiitischen Magmareihe werden als subalkalisch klassifiziert (sie enthalten weniger Natrium als einige andere Basalte) und unterscheiden sich von Gesteinen der kalkalkalischen Magmareihe durch den Redoxzustand des Magmas, aus dem sie kristallisieren (tholeiitische Magmen werden reduziert; alkalische Magmen werden oxidiert)
Wie unterscheidet sich eine kovalente Bindung von einem Ionenbindungsquizlet?

Der Unterschied zwischen einer ionischen und einer kovalenten Bindung besteht darin, dass eine kovalente Bindung entsteht, wenn zwei Atome Elektronen teilen. Ionenbindungen sind Kräfte, die elektrostatische Anziehungskräfte zwischen entgegengesetzt geladenen Ionen zusammenhalten. Ionische Bindungen haben einen Elektronegativitätsunterschied größer oder gleich 2
Wie unterscheidet sich die Form einer Pflanzenzelle von der einer tierischen Zelle?
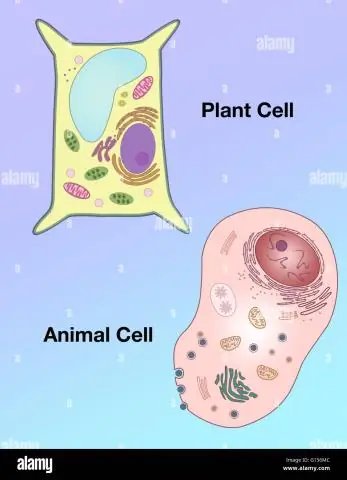
Vakuolen: Pflanzenzellen haben eine große Vakuole, während tierische Zellen mehrere kleine Vakuolen enthalten. Form: Pflanzenzellen haben eine regelmäßigere Form (im Allgemeinen rechteckig), während tierische Zellen unregelmäßige Formen haben. Lysosomen: kommen im Allgemeinen in tierischen Zellen vor, während sie in Pflanzenzellen fehlen
Wie unterscheidet sich eine chemische Veränderung von einem Quizlet zur physikalischen Veränderung?
Was ist der Unterschied zwischen einer chemischen und einer physikalischen Veränderung? Chemische Veränderungen beinhalten die Produktion einer völlig neuen Substanz durch das Aufbrechen und Neuanordnen von Atomen. Physikalische Veränderungen sind normalerweise reversibel und beinhalten nicht die Bildung verschiedener Elemente oder Verbindungen
Wie unterscheidet sich eine Welle von einem Puls?

Beide Begriffe beschreiben Störungen in einem Medium. Welle bezieht sich normalerweise auf eine kontinuierliche Störung. Zum Beispiel, wenn Sie den Frühling greifen und ihn viel hin und her schütteln. Puls hingegen bezieht sich oft auf eine Art einmaliger Störung
