
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Zuletzt bearbeitet 2025-06-01 05:03.
BeCl2 verletzt die Oktettregel . Das Bor muss sich in einem geeigneten Wertigkeitszustand befinden, um an die drei Chlore zu binden. Im Molekül ist das Bor nur mit sechs Elektronen assoziiert. Ein Großteil der Chemie dieses und ähnlicher Moleküle hängt mit der daraus resultierenden starken Elektrophilie zusammen.
Ebenso fragen die Leute, warum Beryllium nicht der Oktettregel folgt?
Beryllium folgt nicht der Oktettregel weil es keine acht Elektronen benötigt, die es umgeben, um stabil zu sein.
Was verstößt ebenfalls gegen die Oktettregel? Dort sind drei Verstöße zum Oktettregel : Moleküle mit ungeraden Elektronen, Moleküle mit Elektronenmangel und Moleküle mit erweiterter Valenzschale.
Verstößt BeH2 in Anbetracht dessen gegen die Oktettregel?
Moleküle, bei denen ein Atom weniger als an. hat Oktett (d. h. BF3, BeH2 , AlCl3). Dies geschieht nur bei Atomen nahe der Grenze zwischen Metallen und Nichtmetallen, wie Be, B, Al und Ga. Elemente in den ersten beiden Perioden, H - Ne, können jedoch nicht gegen die Oktettregel verstoßen auf diese Weise.
Warum kann Schwefel die Oktettregel verletzen?
Zu viele Elektronen: erweitert Oktette Atome in diesen Perioden können dem folgen Oktettregel , aber es gibt Bedingungen, unter denen sie kann erweitern ihre Valenzschalen, um mehr als acht Elektronen aufzunehmen. Schwefeldose Folge dem Oktettregel wie im Molekül SF2. Jedes Atom ist von acht Elektronen umgeben.
Empfohlen:
Warum wird die Molalität gegenüber der Molarität bevorzugt, um die Konzentration einer Lösung auszudrücken?

Die Molarität ist die Anzahl der Mole pro Volumeneinheit der Lösung und die Molarität ist die Anzahl der Mole pro Masseneinheit des Lösungsmittels. Das Volumen ist temperaturabhängig, wobei die Masse bei allen Temperaturen konstant ist. Die Molalität bleibt also konstant, aber die Molarität ändert sich mit der Temperatur. Daher wird die Molalität gegenüber der Molarität bevorzugt
Warum ist die EMF Null, wenn die Spule genau durch die Mitte des Magneten läuft?
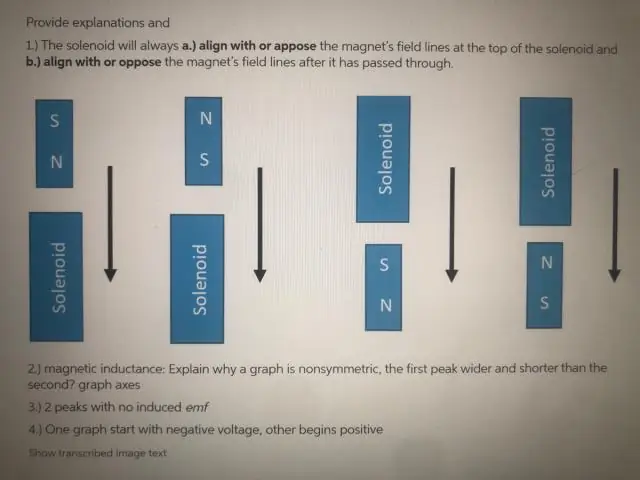
Die EMK ist nur für einen Moment Null, wenn der Magnet genau durch die Mitte der Spule geht. Dies liegt daran, dass die Wirkung des N-Pols am einen Ende des Magneten an diesem Ende der Spule durch die Wirkung des S-Pols des Magneten am anderen Ende der Spule genau aufgehoben wird
Warum beeinflusst die geografische Lage die Menge an Sonnenlicht, die ein Ökosystem erhält?

Warum beeinflusst die geografische Lage die Menge an Sonnenlicht, die ein Ökosystem erhält? Globale Windmuster beeinflussen verschiedene Ökosysteme, weil sie Pollen und Samen verbreiten; beeinflusst Temperatur und Niederschlag; und erzeugt Strömungen in Seen, Bächen und Ozeanen
Verstößt so3 gegen die Oktettregel?

Warum SO3 stabil ist Schwefel bildet ein erweitertes Oktett. Das bedeutet, dass es der Oktettregel nicht wirklich gehorcht, sodass es zusätzliche Elektronen aufnehmen kann. Schwefel ist ein Element der 3. Periode; daher kann es seine 3d-Orbitale verwenden, um mehr als 4 Bindungen einzugehen
Sind elektrisches Potenzial und potenzielle Energie gleich Warum oder warum nicht?

Die elektrische potentielle Energie Ue ist die potentielle Energie, die gespeichert wird, wenn Ladungen aus dem Gleichgewicht geraten (wie die potentielle Gravitationsenergie). Das elektrische Potenzial ist das gleiche, aber pro Ladung Ueq. Eine elektrische Potentialdifferenz zwischen zwei Punkten wird Spannung genannt, V=Ue2q'Ue1q
