- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Zuletzt bearbeitet 2025-01-22 16:55.
Bohrsches Atommodell : 1913 Bohr vorgeschlagen seine quantisierte Schale Modell des Atom zu erklären wie Elektronen kann stabile Umlaufbahnen um den Kern haben. Die Energie eines Elektron hängt von der Größe der Umlaufbahn ab und ist bei kleineren Umlaufbahnen niedriger. Strahlung kann nur auftreten, wenn die Elektron springt von einer Bahn zur anderen.
Wie beschreibt Niels Bohr Elektronen in seinem Atommodell?
Sie umkreisen den Zentralkern auf diskreten Bahnen. Elektronen umkreisen den Kern auf bestimmten, definierten Bahnen. Jeder Pfad hat eine bestimmte Energie.
Außerdem, wie fand Bohr seine Theorie? Atommodell The Bohr Das Modell zeigt das Atom als kleinen, positiv geladenen Kern, der von kreisenden Elektronen umgeben ist. Bohr war der erste, der entdecken dass Elektronen in getrennten Bahnen um den Kern wandern und dass die Anzahl der Elektronen in der äußeren Bahn die Eigenschaften eines Elements bestimmt.
Was erklärt auch das Bohrsche Modell?
Die Bohr-Modell zeigt, dass sich die Elektronen in Atomen auf Bahnen unterschiedlicher Energie um den Kern befinden (man denke an Planeten, die um die Sonne kreisen). Bohr verwendet den Begriff Energieniveaus (oder Schalen), um diese Bahnen unterschiedlicher Energie zu beschreiben.
Wie hat Bohr Rutherfords Atommodell erweitert?
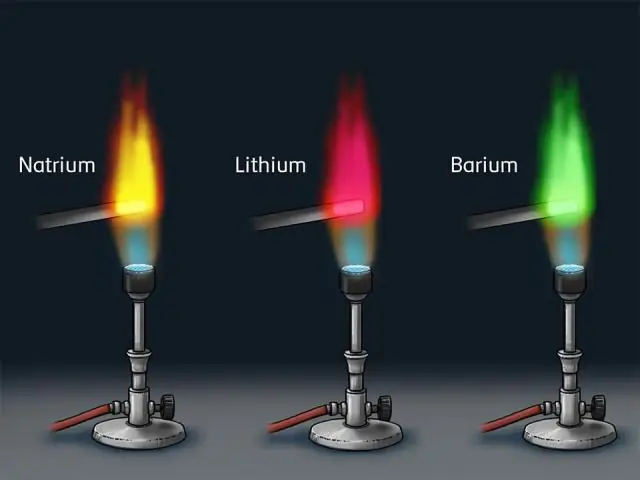
Bohr verbessert Rutherfords Modell indem er vorschlug, dass sich Elektronen in Bahnen mit bestimmten Energieniveaus um den Kern bewegten. Wenn ein Metall Atom erhitzt wird, nimmt es Energie auf und die Elektronen springen auf höhere Energieniveaus.
Empfohlen:
Warum hat Bohr Rutherfords Atommodell überarbeitet?

Bohr-Atommodell: 1913 schlug Bohr sein quantisiertes Schalenmodell des Atoms vor, um zu erklären, wie Elektronen stabile Umlaufbahnen um den Kern haben können. Um das Stabilitätsproblem zu lösen, modifiziert Bohr das Rutherford-Modell, indem er verlangt, dass sich die Elektronen auf Bahnen fester Größe und Energie bewegen
Wie hat Holmes Konvektionsströme beschrieben?

Holmes stellte die Theorie auf, dass sich Konvektionsströme durch den Erdmantel auf die gleiche Weise bewegen, wie erhitzte Luft durch einen Raum zirkuliert, und dabei die Erdoberfläche radikal umgestalten. Holmes verstand auch die Bedeutung der Konvektion als Mechanismus für den Wärmeverlust der Erde und die Kühlung ihres tiefen Inneren
Welche Ordnungszahl hat Germanium, wie viele Elektronen hat Germanium?

Name Germanium Atommasse 72,61 Atommasseneinheit Anzahl der Protonen 32 Anzahl der Neutronen 41 Anzahl der Elektronen 32
Wie hat Bohr Rutherfords Atommodell verbessert?

Bohr verbesserte Rutherfords Atommodell, indem er vorschlug, dass sich Elektronen auf Kreisbahnen mit bestimmten Energieniveaus bewegen. Beschreibung: Rutherford schlug vor, dass Elektronen den Kern wie Planeten um die Sonne umkreisen. Wenn ein Metallatom erhitzt wird, absorbiert es Energie und die Elektronen springen auf höhere Energieniveaus
Wie hat Niels Bohr das Planetenmodell entdeckt?

Bohr-Atommodell: 1913 schlug Bohr sein quantisiertes Schalenmodell des Atoms vor, um zu erklären, wie Elektronen stabile Umlaufbahnen um den Kern haben können. Die Energie eines Elektrons hängt von der Größe der Bahn ab und ist bei kleineren Bahnen geringer. Strahlung kann nur auftreten, wenn das Elektron von einer Bahn in eine andere springt
