
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:32.
- Zuletzt bearbeitet 2025-01-22 16:55.
Die Bildungsenthalpie für ein Element in seinem elementaren Zustand wird es immer sein 0 weil es keine Energie braucht, um eine natürlich vorkommende Verbindung zu bilden. Wenn ein Stoff gebildet von der stabilsten Form seiner Elemente , eine Änderung in Enthalpie stattfinden.
Ebenso kann man fragen, welche Stoffe eine Bildungsenthalpie von Null haben?
Alle Elemente in ihren Standardzuständen (Sauerstoffgas, fest Kohlenstoff in Form von Graphit , etc.) haben eine Standardbildungsenthalpie von Null, da an ihrer Bildung keine Änderung beteiligt ist.
Anschließend stellt sich die Frage, wie groß die Bildungsenthalpie von Wasser ist. Ausgewählte ATcT-Bildungsenthalpie basierend auf Version 1.118 des Thermochemical Network
| Artname | Formel | ΔFH°(298,15 K) |
|---|---|---|
| Wasser | H2O (cr, eq.press.) | -292.740 |
Warum ist dementsprechend die Standardbildungsenthalpie von Diamant nicht Null, obwohl es sich um ein Element handelt?
Die Standardbildungsenthalpie für ein Element in seinem Standard Zustand ist NULL !!!! H°f für C (s, Graphit) ist also Null , aber das ΔH°f für C (s, Diamant ) beträgt 2 kJ/mol. Das liegt daran, dass Graphit das ist Standard Zustand für Kohlenstoff, kein Diamant.
Was bedeutet es, wenn Delta h null ist?
Sie können nur Enthalpieänderungen messen. Wenn die Enthalpie positiv ist und Delta H ist größer als Null , Dies meint dass ein System Wärme absorbiert. Dies wird als endotherme Reaktion bezeichnet. Wenn die Enthalpie negativ ist und Delta H ist weniger als Null , Dies meint dass ein System Wärme freisetzt. Dies wird als exotherme Reaktion bezeichnet.
Empfohlen:
Warum ist die induzierte EMK Null, wenn der magnetische Fluss maximal ist?

Wenn die Spule aufrecht steht, ändert sich der magnetische Fluss nicht (dh EMK = 0), da die Spule die Feldlinien nicht "schneidet". Die induzierte EMK ist Null, wenn die Spulen senkrecht zu den Feldlinien stehen, und maximal, wenn sie parallel sind. Denken Sie daran, dass die induzierte EMK die Änderungsrate der Magnetflussverknüpfung ist
Warum werden das Zerreißen von Papier und das Verbrennen von Papier als zwei Arten von Veränderungen betrachtet?

Das Reißen eines Papiers ist eine physikalische Veränderung, da beim Zerreißen des Papiers nur das Aussehen des Papiers verändert wird und keine neue Substanz gebildet wird. Das Zerreißen von Papier ist eine physikalische Veränderung, weil es gleich bleibt, aber das Verbrennen von Papier ist eine chemische Veränderung, weil es sich in Asche verwandelt
Warum ist die EMF Null, wenn die Spule genau durch die Mitte des Magneten läuft?
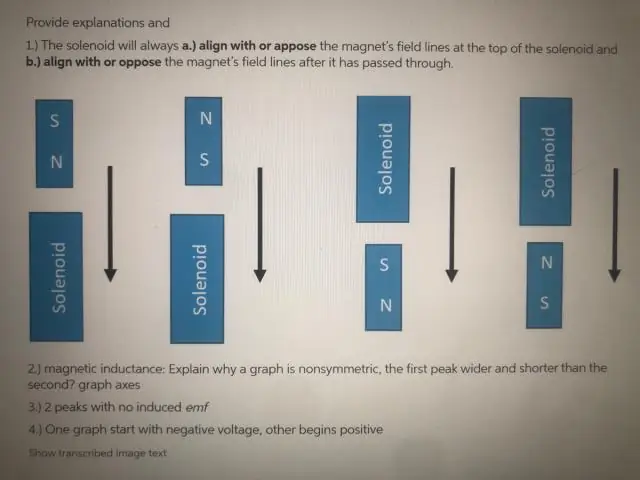
Die EMK ist nur für einen Moment Null, wenn der Magnet genau durch die Mitte der Spule geht. Dies liegt daran, dass die Wirkung des N-Pols am einen Ende des Magneten an diesem Ende der Spule durch die Wirkung des S-Pols des Magneten am anderen Ende der Spule genau aufgehoben wird
Wie groß ist die Bildungsenthalpie von Cao?

Tabelle der Bildungswärmen der Verbindung ΔHf (kJ/mol) CaCO3 -1207,0 CaO(s) -635,5 Ca(OH)2(s) -986,6 CaSO4(s) -1432,7
Was ist die periodische Klassifizierung von Elementen?

Das Periodensystem, auch Periodensystem der Elemente genannt, ist eine tabellarische Darstellung der chemischen Elemente, die nach Ordnungszahl, Elektronenkonfiguration und wiederkehrenden chemischen Eigenschaften geordnet sind. Die als Gruppen bezeichneten Spalten enthalten Elemente mit ähnlichem chemischen Verhalten
