
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:32.
- Zuletzt bearbeitet 2025-01-22 16:55.
Wie verdünnte Schwefelsäure ist ideal für Redox Titration weil es weder ein Oxidationsmittel noch ein Reduktionsmittel ist. HCL ist ein starker Elektrolyt und dissoziiert in Wasser zu H+ und Cl- Ionen. Daher etwas KMnO4 ist Gebraucht oxidiert Cl- zu Cl2. Seite an Seite KMnO4 oxidiert Oxalationen zu CO2.
Die Leute fragen auch, warum h2so4 bei der Titration von KMnO4 verwendet wird.
Schwefelsäure wird hinzugefügt, um eine Hydrolyse zu verhindern und überschüssige H+-Ionen in der Lösung bereitzustellen, um die Reaktion am Laufen zu halten und auch Schwefelsäure ist oxidationsstabil. Aus der obigen Reaktion ist ersichtlich, dass pro Mol MnO4- so. 8 Mol H+-Ionen benötigt werden Schwefelsäure liefert das erforderliche Wasserstoff-Ion.
Wissen Sie auch, warum KMnO4 bei der Titration verwendet wird? Daher KMnO4 fungiert als eigener Indikator. Kaliumpermanganat ist ein Oxidationsmittel von tiefvioletter Farbe. Wann Gebraucht im Redox Titration , wird es am Endpunkt zu braun gefärbten Mn2+-Ionen (in sauren Medien) reduziert und die Farbänderung am Endpunkt kann leicht nachgewiesen werden.
Warum fügen wir in diesem Zusammenhang Dil h2so4 bei der Titration hinzu?
Schwefelsäure ( H2SO4 ) wird im Redox verwendet Titration weil es die H(+)-Ionen liefert, die für eine schnellere Reaktion notwendig sind, während die Sulfat(-)-Ionen während der Reaktion kaum reagieren. Deswegen, Schwefelsäure wird zugegeben, um die Lösung sauer zu machen.
Warum wird HCl bei der KMnO4-Titration nicht verwendet?
KMnO4 ist ein sehr starkes Oxidationsmittel und kann oxidieren HCl Chlorgas freizusetzen, daher HCl kann nicht sein Gebraucht ansäuern Kaliumpermanganat Lösung in der volumetrischen Analyse.
Empfohlen:
Warum wird PCR bei der DNA-Sequenzierung verwendet?

PCR steht für Polymerase Chain Reaction, kurz gesagt, es kopiert DNA sehr schnell millionenfach. Es wird bei der DNA-Sequenzierung verwendet, da die DNA-Probe manchmal zu klein ist. Dies geschieht zum Beispiel bei Tatortbeweisen oder bei sehr alten Proben (z. B. Mumien)
Warum wird Acetocarmin bei der Mitose verwendet?

Acetocarmin wird als Färbemittel verwendet, um die Zellen, die eine Mitose durchlaufen, klar und genau sichtbar zu machen, um eine vereinfachte Beobachtung und Untersuchung der Zellmitose zu ermöglichen. Um Chromosomen so zu färben, dass sie leicht sichtbar sind und wir ihre Morphologie, Struktur und natürlich auch ihre Anzahl in der Metaphase und Anaphase sehen können
Was ist der Zweck von ATP sowohl bei der Zellatmung als auch bei der Photosynthese?
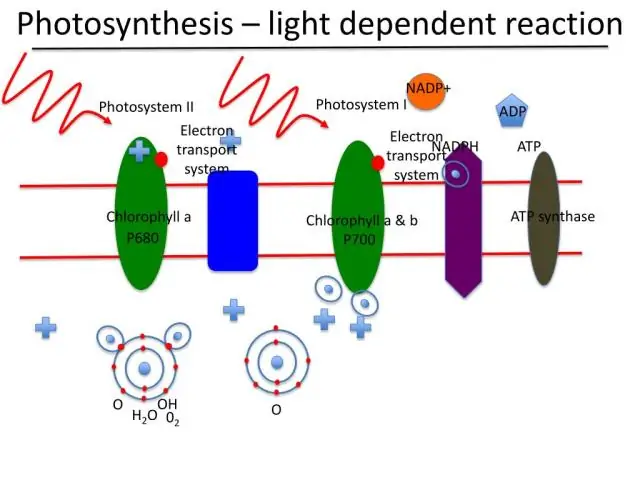
Im Wesentlichen ist es die umgekehrte Reaktion der Photosynthese. Während bei der Photosynthese Kohlendioxid mit Wasser katalysiert durch Sonnenlicht zu Zucker und Sauerstoff reagiert, verwendet die Zellatmung Sauerstoff und spaltet den Zucker unter Bildung von Kohlendioxid und Wasser unter Freisetzung von Wärme und Produktion von ATP . auf
Warum wird Schwefelsäure bei der Redoxtitration verwendet?

Schwefelsäure (H2SO4) wird bei der Redox-Titration verwendet, weil sie die für die Reaktion notwendigen H(+)-Ionen schneller liefert, während die Sulfat(-)-Ionen während der Reaktion kaum reagieren. Daher wird Schwefelsäure hinzugefügt, um die Lösung sauer zu machen
Warum wird Anti-Bumping-Granulat bei der Destillation verwendet?

Zweck der Anti-Stoß-GranulatWatch Sie stoppen das Stoßen, das das plötzliche Auftreten von Dampfblasen in der heißen Flüssigkeit verursacht, die nach oben spritzen. Das Anti-Bumping-Granulat dient als Brennpunkt für die Dampfbildung und ermöglicht ein sanftes Kochen
